超声内镜+微波消融术为胰腺神经内分泌肿瘤实现精准消融
神经内分泌肿瘤是一类相对少见的肿瘤,胰腺是其常见的发病部位。近年来,胰腺神经内分泌肿瘤(pNEN)的发病率明显上升。随着检查技术的进步和健康体检的普及,pNEN的临床检出率亦呈上升趋势。
pNEN起病隐匿,生物学行为呈高度异质性,既可表现为惰性生长,亦可表现为侵袭性生长,甚至早期发生转移。由于大多数病例发现时处于晚期不可切除阶段,已失去了手术干预的机会,为这类患者寻找到安全有效的手术替代方案十分迫切,且势在必行。
病例分享
近日,美国消化内镜学会(ASGE)的官方视频期刊——《GIE》分享了一例超声内镜(EUS)引导下行微波消融术(MWA)治疗胰腺神经内分泌肿瘤的病例。

这是一位72岁的女性患者,患有不可切除的胰腺肿瘤,合并高血压、糖尿病和慢性肾病。10年前,患者曾因肾透明细胞癌行右肾切除术。本次就诊,患者拒绝手术干预,且术前风险指数较高,另外,病变的大小和位置(侵犯脾动脉)也决定了患者无法进行手术治疗,于是医生决定在EUS引导下行MWA治疗。
患者有3个月的非特异性腹痛、体重减轻、恶心等病史。EUS示胰颈部有35×32mm低回声病变,增强EUS见高强化(图1)。随后,在EUS引导下细针穿刺活检证实为胰腺神经内分泌肿瘤。
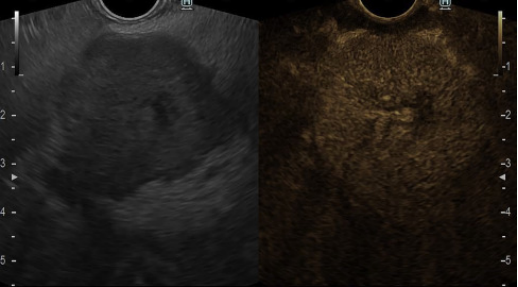
图1 EUS示胰腺颈部35mm×32mm低回声病变,增强扫描呈高强化
使用治疗性线性回声内窥镜进行手术,该内窥镜连接到专用发生器和19.5口径针状天线上,持续传送5.8 GHz信号,持续2分钟,共进行8次,实现了对整个病变区域的完全消融(图2)。
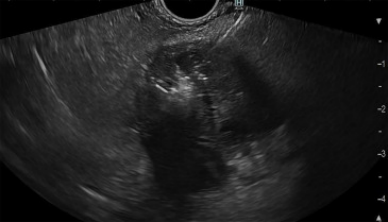
图2 EUS引导下,使用19.5口径针头以5.8 GHz频率对目标肿瘤进行微波消融
完全消融后,在EUS(图3)和MWA后4周的CT平扫(图4)上观察到先前暗部区域变白,病变体积减小。术后4个月随访,患者未发生腹痛或急性胰腺炎。目前,随访已有8个月,术后患者状态良好。
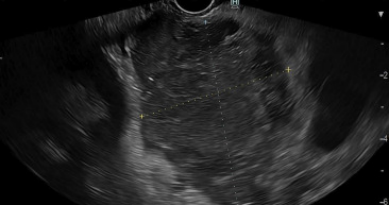
图3 在EUS治疗后,胰颈部病变体积减小
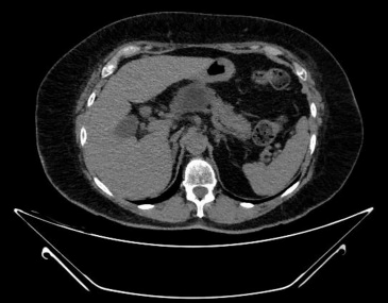
图4 术后4周CT结果,胰头无血管区对应消融区
与RFA相比,MWA更具优势
射频消融(RFA)是常见的微创治疗方式,其原理是利用射频电极针产生射频波在小范围内产生高温,通过热效能使肿瘤凝固性坏死,所以,RFA可能造成不可预测的热损伤风险。相比之下,微波消融(MWA)基于偶极分子振荡产生的摩擦热,可控制并诱导温度上升至90°C,且可提供深层、均匀、一致的能量输送,不会损伤周围组织。
虽然RFA和MWA均实现了凝固性坏死,但后者优势更明显:冷却时间更短,能量传递更有效,对散热器的敏感性更低。此外,MWA不依赖组织阻抗,不受水分蒸发和炭化的限制,不需要电路,成本更低。
EUS+MWA 实现精准消融
MWA将微波天线植入到肿瘤内部,利用其发射出高频的电磁波,造成水分子的旋转摩擦产生热量,利用微波的热效应和肿瘤不耐热的特点,在极短的时间内使肿瘤局部产生高温,促使肿瘤组织发生不可逆凝固性坏死,达到原位灭活肿瘤的目的。在此过程中,EUS引导可提供实时、高质量的成像,实现了治疗的精确定位。
从该病例可以看到,基于其技术优势,EUS引导下MWA是一种更安全的替代方案,其能量分布均匀一致,不会对周围结构或胰腺本身造成损害。此外,MWA可诱导肿瘤细胞死亡,实现精准治疗,而且术后不良事件极少,甚至不存在。因此,它可作为其他治疗方法如化疗、放疗,甚至手术的辅助治疗手段。
总之,EUS引导下MWA是治疗不可切除胰腺神经内分泌肿瘤一种可行、有效、安全的替代方案。
参考资料:
Robles-Medranda Carlos,Arevalo-Mora Martha,Oleas Roberto et al. Novel EUS-guided microwave ablation of an unresectable pancreatic neuroendocrine tumor.[J] .VideoGIE, 2022, 7: 74-76.